Nitrifikation die Stickstoff Umwandlung
Was passiert bei der Nitrifikation
Die Nitrifikation ist die Umwandlung von Ammonium zum Nitrat. Die Nitrifikation erfolgt durch zwei extrem stark spezialisierte Bakterienarten «Nitrosomonas» und «Nitrobacter». Für den Zellaufbau nutzen diese zwei Bakterien nicht organischer Kohlenstoff, sondern das Kohlenstoffdioxid CO 2. Die zum Wachstum notwendige Energie wird aus der Oxidation, des Ammoniums über Nitrit zu Nitrat, bezogen. Die Nitrat Bildung läuft schneller ab als die Nitrit Bildung, so dass Nitrit meist nur in geringer Konzentration vorliegt. An erhöhten Nitrit Konzentration lässt sich eine Beeinträchtigung der Nitrifikation erkennen.
1. Schritt Nitrifikation: Ablauf Oxidation vom Ammonium zum ⇒ Nitrit «Nitrosomonas»
Die Ammonium Oxidierer »Nitrosomonas» wandeln durch bakterielle Oxidation Ammonium zum Nitrit um.

Nitrifikation Abbau
des Ammonium zum Nitrit
2. Schritt Nitrifikation: Ablauf Oxidation vom Nitrit zum ⇒ Nitrat «Nitrobacter»
Die Nitrit Oxidierer «Nitrobacter» oxidieren das entstandene Nitrit weiter zum Endprodukt Nitrat. Ammonium und Nitrit wirken als Elektronen Spender.
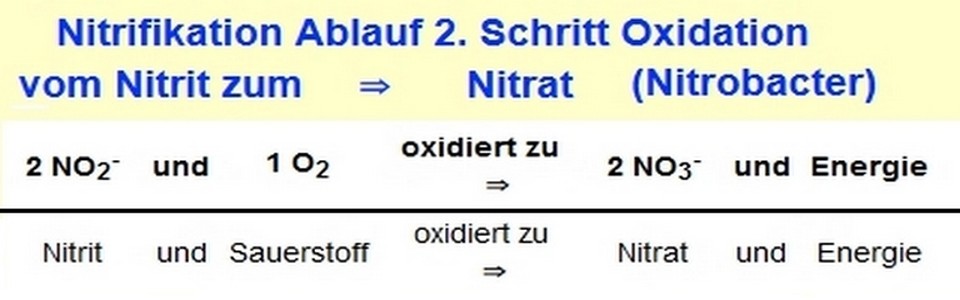
Nitrifikation Abbau
des Nitrit zum Nitrat
Prozessbeschreibung
Die Nitrifikation ist eine Reaktion mit sehr hohem Sauerstoffbedarf. Dieser wird von Aussen als Luftsauerstoff zugeführt. Die Nitrifikanten gehören zu den aeroben Bakterien, weil sie den Sauerstoff als Elektronen Akzeptor benötigen. Als Kohlenstoffquelle nutzen sie organisches Kohlendioxid. Eine schnelle Umwandlung der Nitritsalze durch die Bakterien ist lebensnotwendig, da Nitrit für höhere Pflanzen bei niedrigem pH-Wert fischgiftig wirkt.
Beim Betrieb von Nitrifikations Anlagen ist zu beachten, dass immer nur die nicht ionische Form der Stickstoffverbindungen «Ammoniak,» «salpetrige Säure» als Elektronen Donator verwendet werden kann. Das Verhältnis zwischen den ionischen und nicht ionischen Formen der Verbindungen ist vom pH-Wert abhängig. Dies wird auch durch den Prozess selbst beeinflusst und Bedarf unter Umständen einer pH-Wert Regelung. Im Zuge der Ammonium Oxidation H+ werden Ionen frei und damit steigt die Gefahr einer Senkung des pH-Werts.
Nitrifikanten
Nitrobakterien, Bakterien, mit denen die Nitrifikation erfolgt. Zu den Nitrobakterien zählen einerseits die Nitratbakterien und andererseits die Nitritbakterien. Die bekanntesten Nitrifikanten sind Nitrobacter, eine Gattung Nitrat Bildender Bakterien und Nitrosomonas, eine Gattung Nitrit bildender Bakterien. Nitrobacter und Nitrosomonas, im Boden und im Wasser lebend, ernähren sich autotroph unter Ausnutzung von Energie, die durch Nitrifikation gewonnen wird. Bedingt durch ihre geringen Wachstumsraten ist es notwendig besondere Milieu Bedingungen zu gewährleisten, um diese Bakterien im Abwasser Bereich effektiv einsetzen zu können zur Nitrifikation.
Der in zwei Stufen untergliederte Nitrifikationsprozess kann folgendermassen beschrieben werden:
1. Stufe: Oxidation des Ammonium zu Nitrit.
Dazu muss zuerst die Umwandlung des Ammonium Ions über die vom Enzym Ammonium Mono Oxigenase (AMO) katalysierte Reaktion zum Hydroxylamin erfolgen. Im Anschluss daran wird das gebildete Hydroxylamin durch die Hydroxyl Aminoxid Oreduktase (HAO) in das Endprodukt der ersten Stufe, das Nitrit, umgebaut.
Diese beiden Reaktionsschritte führen Bakterien aus, die allgemein als Ammonium Oxidanten bezeichnet werden. Der bekannteste Vertreter dieser Gruppe ist Nitrosomonas, weshalb dieser immer genannt wird. Die Nitrit oxidierenden Bakterienstämme sind von den Ammonium oxidierern abhängig, da diese durch die Nitritbildung die Lebens Grundlage für die Nitrit oxidierer bilden.
2. Stufe: Oxidation des Nitrits zu Nitrat.
In der zweiten Stufe erfolgt die Umwandlung des entstandenen Nitrit Stickstoffs in seine höhere Oxidationsstufe, dem Nitrat. Repräsentativer Mikroorganismus dieses Schritts ist Nitrobacter.
Bei dieser Reaktion werden Elektronen auf den beteiligten Sauerstoff durch Cytochrom übertragen. Dieser Stoff wirkt als Redoxsystem und dient dem Transport von Elektronen in die Atmungskette der beteiligten Bakterien.
Beide Schritte zusammen werden als Nitrifikation bezeichnet. Dabei nutzen die beteiligten Mikroorganismen die Ausgangsverbindungen Ammonium bzw. Nitrit zur Veratmung mit Sauerstoff. Bei den Reaktionen erfolgt ein Energiegewinn durch Abgabe von Elektronen. Durch die Oxidation der beiden Elektronen Donatoren (Ammonium und Nitrit) werden hierbei Reduktions Gleichwerte (Äquivalente) bereitgestellt. Diese werden über die im Mikro Organismus befindliche Elektronen Transportkette für die Neusynthese von Zellprodukten und Energie verbrauende Prozesse verwendet.
Man rechnet für normales kommunales Abwasser mit einer spezifischen Gesamtstickstoff Fracht von 12 g N / Einwohner und Tag. Etwa 2g davon werden im Rahmen der biologischen Reinigungsprozesse zum Aufbau neuer Biomasse verbraucht. Es bleiben so zirka 10 g N / Einwohner und Tag, die mit der Nitrifikation oxidiert werden müssen.
Wenn die Bedingungen für die Nitrifikation erfüllt sind, wird für die Nitrifikation ein Sauerstoffbedarf von zirka 4.33g O2 pro g Nitrat NO 3 - benötigt.
Die Nitrifikaten Biomasse wächst im Ausmass von 0.24 g CSB je g Nitrat NO 3 - an.
Die technischen Probleme
Die Abwasser technischen Probleme der mikrobiellen Ammonium Oxidation «Nitrifikation» sind im Wesentlichen auf die biologischen Eigenheiten der nitrifizierenden Bakterien zurückzuführen. Im Vordergrund steht dabei die Tatsache, dass diese Organismen im Vergleich zu den heterotrophen Bakterien nur eine überaus geringe Vermehrungsrate haben. Die Generations Zeit der heterotrophen Bakterien liegt bei zirka 2 Stunden, die der Nitrifikanten bei zirka 12 Stunden. In diesen Fällen steht den Nitrifikanten im Wasserkörper nicht genug Zeit zur Verfügung, um sich zu einer hinreichend leistungsfähigen nitrifizierenden Bakterien Population zu entwickeln. Infolge der laufenden Ausspülung der Nitrifikanten stellt sich im biologischen Reaktions Raum ein Gleich Gewicht zwischen Vermehrung und Ausschwemmung auf einem so niedrigen Niveau ein, dass die relativ wenigen im Abwasser flottierenden Nitrifikanten nur geringfügig zu Stickstoffoxidation beitragen können. Unter diesen Bedingungen hängt die Nitrifikationsleistung überwiegend von den am Teichboden fest sitzenden Nitrifikanten ab. Die Immobilisation von Nitrifikanten auf Festkörpern wird unter anderen auch in Biofiltern als auch Hochleistungsreaktoren zur Stickstoffelimination ausgenutzt. Für die Stickstoffelimination ist neben der Nitrifikation der weitere Schritt Denitrifikation notwendig.
Die Nitrifikation ist unter anderem abhängig von
-
Temperatur:
- Ist die Temperatur kleiner als 5 °C findet keine Nitrifikation statt
- Die Nitrifikation wird bei Temperaturen unter 12 °C verlangsamt und unter 8 °C eingestellt.
- Das Optimum liegt zwischen 28 - 36 °C -
Gelöste Sauerstoff Konzentration:
- muss > = 2 mg O2/l betragen. -
pH-Wert und Pufferkapazität:
- starke Abhängigkeit, optimaler Bereich pH-Wert = 7.5 - 8.3 -
Organische Belastung
-
Relevante Substrat Konzentrationen:
- Ammonium, Nitrit, Nitrat -
Spurenstoff Versorgung
-
Eventuelles Vorhandensein von Hemmstoffe:
(Fettlösende Substanzen, Giftstoffe) -
Kontaktzeit zwischen nitrifizierender Biomasse und Abwasser:
Schlammalter 8 - 12 Tage





